Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

A
Dung dịch X. Số mol (SO4)2- = 0,03 mol.
Từ pH = 2 ta tính được số mol H+ = 5. 10-3 mol.
Vậy số mol H+ trong dung dịch Y là : 0,01 + 5. 10-3 = 0,015 mol
Số mol của Ba2+ = 2,5.10-3 mol.
Ba2+ + SO42- ® BaSO4
Vậy khối lượng kết tủa: m = 2,5.10-3.233 = 0,5825 gam.

Đáp án C
+ N a + : 0 , 12 N H 4 + : 0 , 05 C l - : 0 , 12 S O 4 2 - : x = 0 , 025 ⏟ d u n g d ị c h X + B a 2 + : 0 , 03 O H - : 0 , 06 l → B a S O 4 : 0 , 025 N H 3 : 0 , 05 + N a + : 0 , 12 l C l - : 0 , 12 B a 2 + : 0 , 005 O H - : 0 , 01 ⏟ d u n g d ị c h Y + Y → c ô c ạ n m c h ấ t r ắ n = m i o n = 7 , 875 g a m

Đáp án A
Theo BTĐT: x = (0,12 + 0,05 – 0,12) : 2 = 0,025 mol.
Cho 0,03 mol Ba(OH)2 phản ứng với ddX
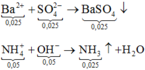
Vậy khi phản ứng xảy ra hoàn toàn, lọc bỏ kết tủa thu được ddY gồm 0,12 mol Na+; 0,12 mol Cl−; 0,005 mol Ba2+; 0,01 mol OH−
Vậy m = 0,12x23 + 0,12x35,5 + 0,005x137 + 0,01x17 = 7,875 gam

Chọn C
Bảo toàn điện tích đối với dung dịch X, ta có: 0,07.1 = 0,02.2 + x.1 → x = 0,03
Bảo toàn điện tích đối với dung dịch Y, ta có: y.1 = 0,04.1 ⇒ y = 0,04
Khi trộn dung dịch X và Y thì H+ + OH- → H2O
(0,04) (0,03)
⇒ nH+còn dư = 0,04 – 0,03 = 0,01 mol ⇒ [H+] còn dư = 0,01/0,1 = 0,1M ⇒ pH = – lg[H+] = 1

Đáp án C
Số mol nHCl = 0,04 mol ⇒ nOH– = 0,04 mo.
⇒ Bảo toàn điện tích ta có: nNa+ = 0,03 mol.
⇒ Chất rắn thu được khi cô cạn dd X = 0,01×137 + 0,01×62 + 0,04×17 + 0,03×23 = 3,36 gam

Đáp án : D
Bảo toàn điện tích : 3a + 0,15 = b + 0,06
nOH = 0,252 mol ; n B a 2 + = 0,018 mol < n S O 4
=> kết tủa gồm 0,018 mol BaSO4 và Al(OH)3
=> n A l O H 3 = 0,018 mol < 1 3 nOH
=> có hiện tượng hòa tan kết tủa
=> n A l O H 3 = 4 n A l 3 + - n O H - n H +
=> n A l 3 + = a = 0,03 mol
=> b = 0,18 mol
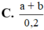


Ta có OH- 0,06 mol và H+ có 0,05 mol
=> Sau khi trộn còn dư 0,01 mol OH- và V = 1 lít
=> pH = 12
=> Đáp án B